D) тяжелый ионный луч и протонная терапия

Тяжелый ионный луч и Центр протонной терапии (вместе): MedAustron в Винер-Нойштадте (Австрия) 
Центр ионного ина MedAustron в Австрии: самая дорогая и современная машина облучения в мире. 
Тяжелый ионный центр в университетской больнице Марбурга (Германия) 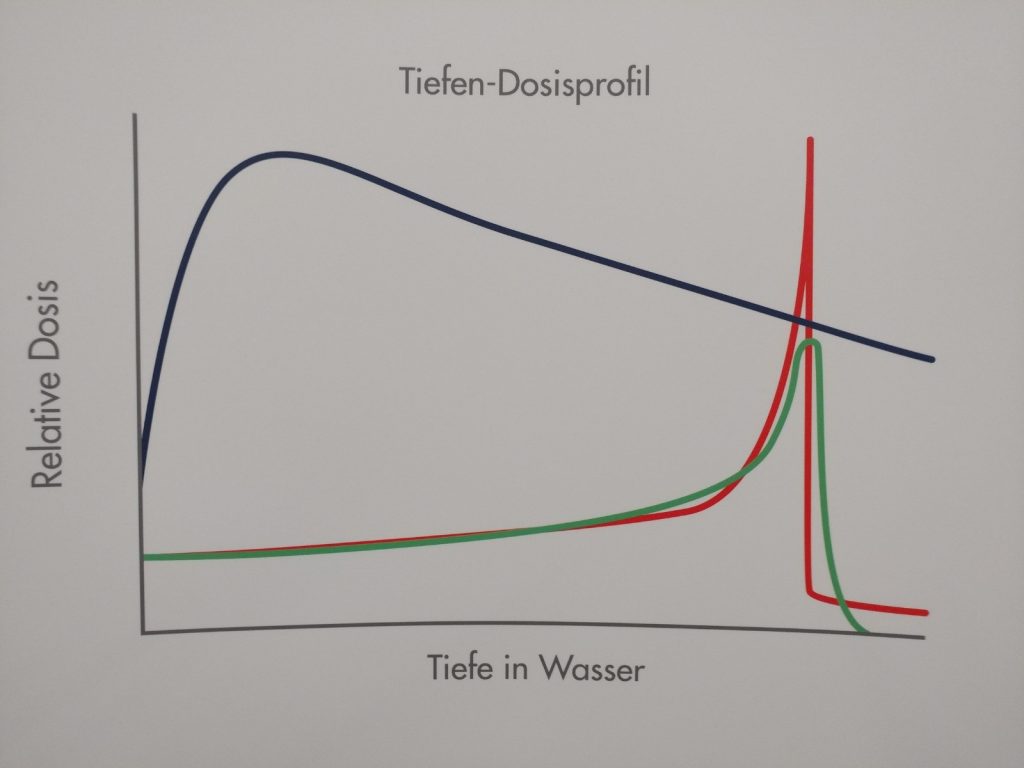
Разрушительная сила тяжелого ионного излучения против рака более чем в два раза превышает протонную радиацию.
Важное уведомление!
В соответствии с международным соглашением об этике, тяжелое ионное излучение может быть использовано только в лечебном смысле, а не в паллиативном смысле. В случае слабых или не четко узнаваемых метастазов, тяжелое ионное излучение может быть использовано, если излучение используется для обеспечения дальнейших хирургических мер радиации или для продления срока службы значительно и качественно.
1) карциномы легких (MedAustron), 2) рак молочной железы, 3) рак поджелудочной железы, 4) карциномы печени (терапия показаний в MedAustron в Австрии, например): https://www.netdoktor.at/therapie/ionentherapie-6926660
Для точного лечения опухоли используется обратный профиль дозы глубины протонов или ионов углерода. Опухолевые клетки умирают, если их клеточная ДНК непоправимо уничтожена и деление клеток больше невозможно. Частица терапии использует обратный профиль дозы глубины протонов или ионов углерода для точного лечения опухоли. Опухолевые клетки умирают, если их клеточная ДНК непоправимо уничтожена и деление клеток больше невозможно.
Протоны, используемые в ионной терапии, являются положительно заряженными ядрами атомов водорода. Они имеют различный физический характер взаимодействия с тканью по сравнению с обычной фотон лучевой терапии (гамма-излучение, рентгеновские лучи) или электронов.
Из-за защиты нормальной ткани, ионная терапия также может быть использована для более высоких доз облучения. Другое лечение ионной терапии является то, что с ионами углерода. Они имеют примерно в три раза более высокую биологическую активность, чем протоны.
Радиация сконцентрирована именно на больной ткани, а нормальная ткань в значительной степени опущена или загружена только с низкой дозой.
Перспективные исследования показали, что даже опухоли, которые в значительной степени устойчивы к обычной лучевой терапии, во многих случаях поддается лечению. Это придаст борьбе с раком новое, обнадеживающее измерение. Поэтому ионная терапия углерода особенно подходит для опухолей костей и мягких тканей вблизи радиопаковых органов, медленно растущих опухолей, опухолей с низким содержанием кислорода или локальных рецидивов после обычной лучевой терапии.
Перспективные исследования показали, что даже опухоли, которые в значительной степени устойчивы к обычной лучевой терапии, во многих случаях поддается лечению. Это придаст борьбе с раком новое, обнадеживающее измерение. Частица терапии использует обратный профиль дозы глубины протонов или ионов углерода для точного лечения опухоли.

ускоритель частиц (MedAustron: Австралия) против рака легких 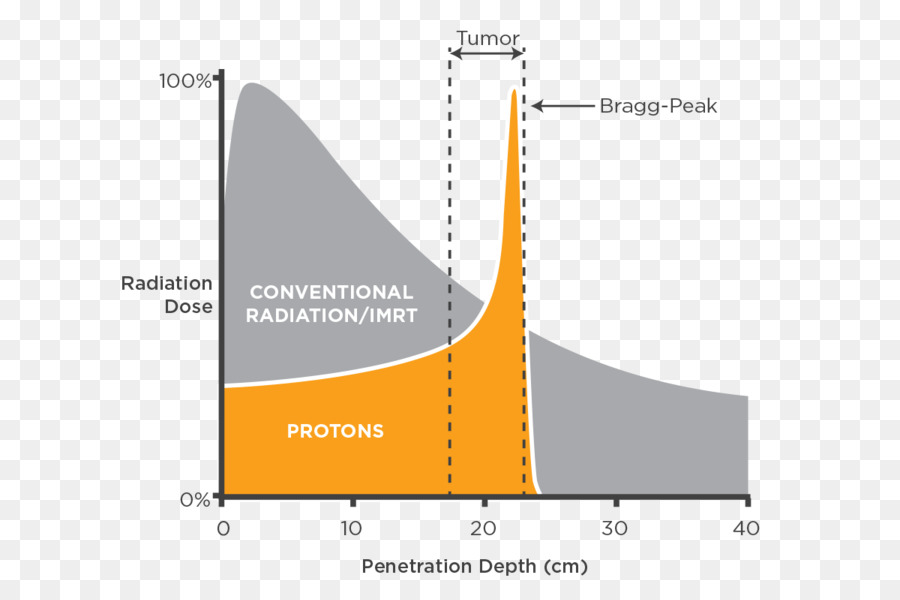
"Брэгг пиккривая" 
медицинский директор MedAustro
nProf. Доктор Евгени
й Хуг, ведущий ученый в мире по терапии частиц
Д-р Пьеро Фоссати: Пионер тяжелой ионной терапии (MedAustron)
В отличие от (обычных) фотонных лучей, доза которых является самой высокой вскоре после проникновения в ткани, а затем снова падает, пучки частиц высвобождают свою основную дозу только ближе к концу своей орбиты в так называемом "Пике Брэгга".
"Bragg пик" является выраженным пиком на "Брэгг кривой", которая графики потери энергии ионизирующего излучения во время его путешествия через материю. Для протонов, лучей и других ионных лучей пик наступает непосредственно перед тем, как частицы упираются в покой. Это называется пик Брэгг, после Уильям Генри Брэгг, который открыл его в 1903 году.
Явление используется в частичной терапии рака, чтобы сконцентрировать влияние световых ионных лучей на лечение опухоли при минимизации воздействия на окружающие здоровые ткани.
Расположение «Вершины Брэгга» может быть точно скорректировано энергией, используемой для ускорения частиц. Это делается с помощью энергетического переменного ускорителя, синхротрона. Диапазон, фокус и интенсивность пучка частиц точно регулируется для лечения опухолевой ткани с миллиметровой точностью.
Основой для планирования лечения является трехмерная реконструкция опухоли, которая делится на отдельные слои различной глубины. Обработка унесена слой за слоем, whereby глубина проникания пучка частицы проконтролирована энергией произведенной в синхротроне.
Опухолевые клетки умирают, если их клеточная ДНК непоправимо уничтожена и деление клеток больше невозможно. Клетки обладают мощными механизмами для восстановления радиационного повреждения, вероятность ремонта зависит от так называемой плотности повреждения.
Протоны и ионы углерода поражают электроны из атомов, с которыми они сталкиваются по пути через ткани (ионизация). В отличие от (обычных) фотонных лучей, доза которых является самой высокой вскоре после проникновения в ткани, а затем снова падает, лучи частиц высвобождают свою основную дозу только ближе к концу своей орбиты в так называемом "Пике Брэгга".
"Bragg пик" является выраженным пиком на "Брэгг кривой", которая графики потери энергии ионизирующего излучения во время его путешествия через материю. Для протонов, лучей и других ионных лучей пик наступает непосредственно перед тем, как частицы упираются в покой. Это называется пик Брэгг, после Уильям Генри Брэгг, который открыл его в 1903 году.
Явление используется в частичной терапии рака, чтобы сконцентрировать влияние световых ионных лучей на лечение опухоли при минимизации воздействия на окружающие здоровые ткани. Расположение "Bragg Peak" может быть точно скорректировано энергией, используемой для ускорения частиц. Это делается с помощью энергетического переменного ускорителя, синхротрона. Диапазон, фокус и интенсивность пучка частиц точно регулируется для лечения опухолевой ткани с миллиметровой точностью.
Основой для планирования лечения является трехмерная реконструкция опухоли, которая делится на отдельные слои различной глубины. Обработка унесена слой за слоем, whereby глубина проникания пучка частицы проконтролирована энергией произведенной в синхротроне.
Опухолевые клетки умирают, если их клеточная ДНК непоправимо уничтожена и деление клеток больше невозможно. Клетки обладают мощными механизмами для восстановления радиационного повреждения, вероятность ремонта зависит от так называемой плотности повреждения. Протоны и ионы углерода поражают электроны из атомов, с которыми они сталкиваются по пути через ткани (ионизация).